ऊष्मागतिक साम्य [Thermodynamic Equilibrium] और ऊष्मागतिक प्रक्रम से संबंधित सभी महत्वपूर्ण जानकारी दी गई है।
निम्न ऊष्मागतिक के टॉपिक की सभी महत्वपूर्ण जानकारी नीचे दी गयी है
- ऊष्मागतिक साम्य ( Thermodynamic Equilibrium )
- ऊष्मागतिक प्रक्रम ( Thermodynamic Process )
ऊष्मागतिक साम्य ( Thermodynamic Equilibrium )
जब किसी निकाय के स्थूल गुण जैसे दाब , ताप इत्यादि में समय के साथ कोई परिवर्तन नहीं होता तो वह तंत्र ऊष्मागतिक साम्य में होता है ।
ऊष्मागतिक साम्य में तीन प्रकार के साम्य निहित होते हैं
- रासायनिक साम्य
- यांत्रिक साम्य
- तापीय साम्य
( i ) रासायनिक साम्य – वह साम्य जिसमें समय के साथ विभिन्न प्रावस्थाओं का संघटन अपरिवर्तित रहता है अर्थात् पदार्थों की सान्द्रताओं में कोई परिवर्तन नहीं होता , उसे रासायनिक साम्य कहते हैं ।
( ii ) यांत्रिक साम्य – वह साम्य जिसमें तंत्र का एक भाग , दूसरे भाग पर कोई यांत्रिक कार्य नहीं करता है उसे यांत्रिक साम्य कहते हैं । यांत्रिक साम्य में पूरे निकाय में दाब समान रहता है ।
( iii ) तापीय साम्य – वह तंत्र जिसके सभी भागों का ताप समान होता है तो वह तंत्र तापीय साम्य में होता है । तापीय साम्य में तंत्र के एक भाग से दूसरे भाग में ऊष्मा का प्रवाह नहीं होता है ।
कक्षा 11 रसायन विज्ञान नोट्स Chemistry Notes
ऊष्मागतिक प्रक्रम ( Thermodynamic Process )
वह प्रक्रिया जिसके द्वारा किसी निकाय की अवस्था में होता है उसे ऊष्मागतिक प्रक्रम कहते हैं ।
निकाय की अवस्था में परिवर्तन निम्नलिखित प्रक्रमों द्वारा किया जा सकता है
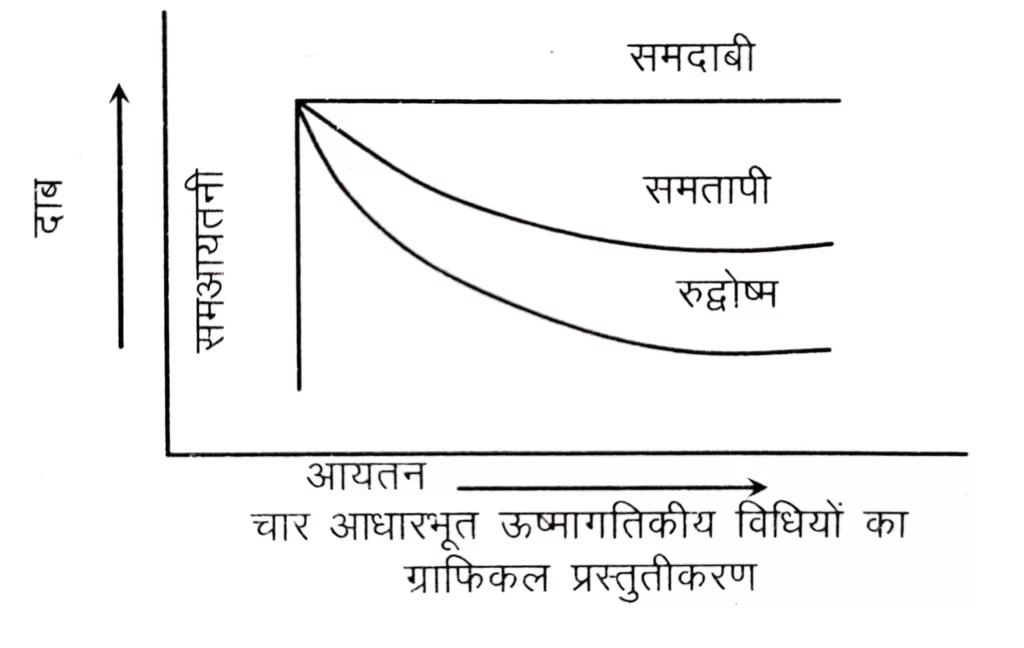
( i ) समतापीय प्रक्रम ( Isothermal process ) : इस प्रक्रम को समतापी इसलिये कहते हैं , क्योंकि इसमें ताप स्थिर रहता है , अर्थात् प्रचालन ( Operation ) स्थिर ताप पर किया गया है ।
समतापी प्रक्रम के लिये dT = 0 , अतः AE = 0
( ii ) रुद्घोष्म प्रक्रम ( Adiabatic process ) : यदि प्रक्रम ऐसी परिस्थितियों में होता है कि तंत्र तथा उसके वातावरण में ऊष्मा का कोई विनिमय नहीं हो पाता है ; तो वह रूद्घोष्म प्रक्रम कहलाता है ।
निकाय ऊष्मीय विलगित ( Thermally isolated ) होता है अर्थात् dQ =0 , यह निकाय को रोधी पात्र में रखकर किया जा सकता है , अर्थात् थर्मस फ्लास्क में ।
( iii ) समदाबीय प्रक्रम ( Isobaric process ) : वह प्रक्रम जिसमें दाब सम्पूर्ण परिवर्तन के दौरान हमेशा स्थिर रहता है , अर्थात् dP=0 समदाबीय प्रक्रम कहलाता है ।
( iv ) समआयतनिक प्रक्रम ( Isochoric process ) : वह प्रक्रम जिसमें सम्पूर्ण परिवर्तन के दौरान आयतन हमेशा स्थिर रहता है , अर्थात् dV = 0 , समआयतनिक प्रक्रम कहलाता है ।
( v ) चक्रीय प्रक्रम ( Cyclic process ) : जब तंत्र अनेक प्रक्रमों से होता हुआ अपनी प्रारम्भिक अवस्था में आ जाता है तो इसे चक्रीय प्रक्रम कहते हैं , इसमें dE = 0 तथा dH = 0 होता है ।
( vi ) उत्क्रमणीय प्रक्रम ( Reversible process ) : उत्क्रमणीय प्रक्रम वह होता है , जिसमें विपरीत परिवर्तन इस प्रकार से होते हैं कि अग्र प्रक्रम के किसी भाग में हुए सभी परिवर्तन , प्रतीप प्रक्रम में पूर्ण रूप से विपरीत हो जाते हैं , तथा परिवेश या प्रक्रम में भाग ले रही किसी भी वस्तु में कोई परिवर्तन शेष नहीं रहता है ।
( vii ) अनुत्क्रमणीय प्रक्रम ( Irreversible process ) : जब प्रक्रम एक ही पद में प्रारम्भिक अवस्था से अन्तिम अवस्था में घटित होता है और यह स्वतः उत्क्रमित नहीं होता है , तो इसे अनुत्क्रमणीय प्रक्रम कहते हैं अनुत्क्रमणीय प्रक्रम में एण्ट्रॉपी की मात्रा बढ़ती है । अनुत्क्रमणीय प्रक्रम , स्वतः प्रकृति का होता है । सभी प्राकृतिक प्रक्रम अनुत्क्रमणीय प्रकृति के होते हैं ।
